疯狂打call的甲亢造模工具—重组腺病毒Ad-TSHR289,了解一下!
甲亢是一种常见的器官特异性自身免疫性疾病,是由于甲状腺合成释放过多的甲状腺激素,造成机体代谢亢进和交感神经兴奋。甲亢病因很多,与情绪,碘营养,自身免疫,家族遗传性都有关系,常见的有弥漫性毒性甲状腺肿(又称Graves’ disease,GD)、炎性甲亢、药物致甲亢、HCG相关性甲亢和垂体TSH瘤甲亢,其中以Graves甲亢最为常见,约占所有甲亢的60%~80% 。
Graves甲亢每年发病率约为万分之四,其发病关键是在环境与遗传因素的相互作用下,机体免疫系统产生了针对促甲状腺激素受体 (TSHR) 的自身抗体(TSAb),TSAb与TSHR的结合激活下游信号级联反应,模仿TSH持续刺激的效果,从而导致甲状腺功能亢进,若不及时治疗,会导致高发病率和死亡率。此外,Graves甲亢相关眼病折磨着大约50%的患者,尤其难以治疗。
1、促甲状腺激素受体(TSHR)
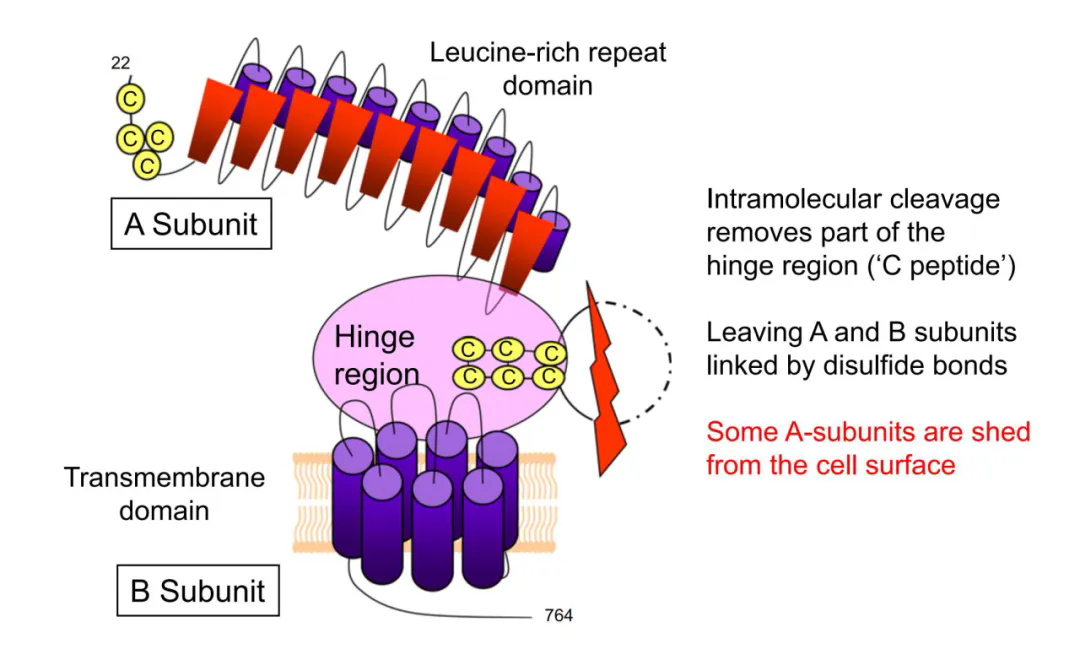
TSHR是一种细胞表面糖蛋白受体,属于G蛋白偶联受体(GPCR)家族成员,由764个氨基酸组成,分子量为87kDa。人类TSHR编码基因位于14号染色体长臂(14q31),基因共含10个外显子,前九个外显子编码胞外庞大的N-端区,该胞外区包含一个富含亮氨酸的重复结构域,通过铰链区与跨膜结构域相连;第十个外显子则编码七个跨膜片段以及胞内短小的C-末端。不同于其他糖蛋白激素受体,TSHR胞外结构域中插入了一个包含50个氨基酸的序列(C肽),在翻译后修饰过程中,金属蛋白酶介导的分子内裂解作用使TSHR的N-端胞外结构域与跨膜螺旋结构域分离,C肽序列被移除,使TSHR转化为通过二硫键连接的A亚基(289aa)和B亚基。
TSHR基因组结构示意图
TSHR蛋白结构示意图
2、TSHR自身抗体(TRAb)
TRAb是一种甲状腺自身抗体,能特异性地针对甲状腺细胞膜表面的TSHR。根据生理学作用的不同,可将TRAb分为甲状腺刺激性抗体(TSAb)及甲状腺刺激阻断抗体(TBAb)。TSAb存在于Graves病患者的血清中,与TSHR结合产生类似TSH的生物效应,刺激甲状腺发生甲亢,是目前GD的首选筛查方法;TBAb存在于自身免疫甲状腺炎甲减患者,可以与TSHR结合,阻断TSH的作用,发生甲减。
3、GD的发病机制
TSHR主要在甲状腺细胞中表达,天然配体是TSH。生理状态下,TSHR胞外结构域抑制跨膜螺旋结构域的活性,当胞外结构域被TSH特异性结合,其构象改变转化为跨膜螺旋结构域的激动剂,从而导致TSHR激活,并引起下游细胞内信号级联反应,以控制甲状腺生长以及甲状腺激素的合成与分泌。病理条件下,TSHR结构发生异常改变,在酶解作用下连接A、B两个亚基的二硫键发生溶解断裂,TSHR-A亚基脱落表达于细胞表面,诱发并增强自身免疫反应,使TSHR作为自身抗原激发机体产生抗体TSAb从而导致甲亢的发生。因此,具有免疫原性的TSHR-A亚基是诱发自身免疫反应的关键,针对TSHR-A亚基的研究成为GD模型研究的热点。
4、GD动物造模方法
目前GD发病机制尚不明确,建立符合GD发病特点的动物模型,对疾病的诊断及治疗研究都具有重要意义。外源性甲状腺素补充法和免疫诱导甲状腺肿是建立诱发性甲亢动物模型的主要方法,其中以表达人TSHR-A亚基的重组腺病毒( Ad-TSHR-289) 免疫诱导的甲亢模型是较为理想且使用广泛的GD动物模型。
参考案例
The thyrotropin receptor autoantigen in Graves disease is the culprit as well as the victim(The Journal of Clinical Investigation,IF 15.9)
实验方法
① 腺病毒表达载体的构建及体内注射
研究者分别构建了编码TSHR游离A亚基(TSHR-289)和TSHR全长(TSHR-D1NET,经历最小程度的亚基切割)的腺病毒,并以Ad-β-gal及Ad-TSHR-WT作为对照。将上述腺病毒肌肉注射至6-7周龄雌性BALB/c小鼠,病毒用量为1011 particles,注射体积为50μL PBS混悬液。
腺病毒装载的三种不同结构形式的TSHR
② 腺病毒免疫方法
腺病毒注射小鼠三次,且每次间隔三周,并在第二次注射后1周抽血,在第三次注射后8周(第一次实验)或4周(第二次实验)对动物实施安乐死,以获得血液和甲状腺。
实验结果
二次免疫后血清甲状腺素水平检测显示Ad-TSHR-289组有80%的小鼠T4水平增高,而Ad-TSHR-D1NET组仅为10% ; 三次免疫后的检测得到了类似的结果。组织学检查显示90%的Ad-TSHR-289免疫小鼠表现出明显的甲状腺肿,而Ad-TSHR-D1NET免疫小鼠仅有20%出现甲状腺肿。Ad-TSHR-WT免疫的小鼠表现了介于两者之间的反应。
TSHR腺病毒注射小鼠的甲状腺肿和组织学比较
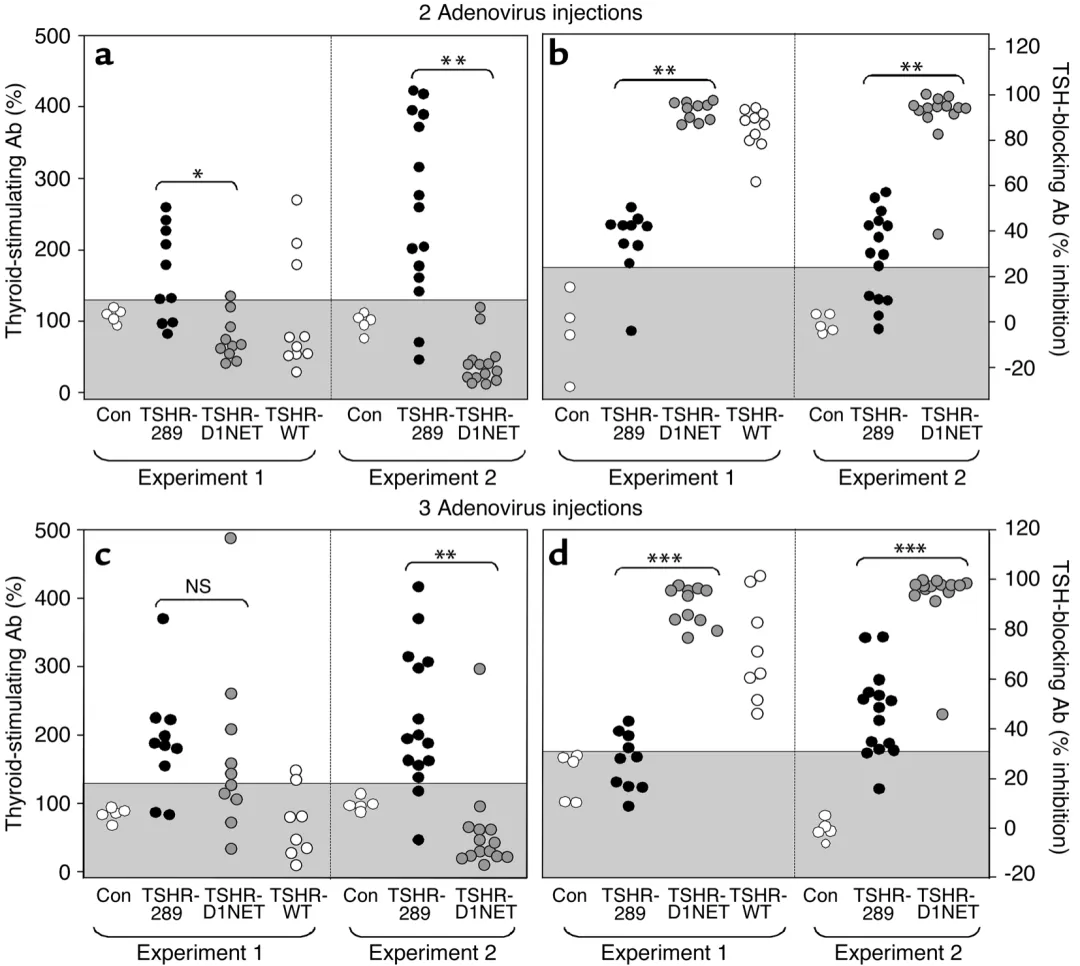
cAMP反应测定数据显示二次免疫后Ad-TSHR-289组小鼠血清中的TSAb活性明显高于Ad-TSHR-D1NET组,而TBAb活性则显著低于Ad-TSHR-D1NET组,Ad-TSHR-WT组TSAb和TBAb水平介于二者之间。
表达不同结构形式TSHR的腺病毒免疫的小鼠中的TSAb和TBAb
以上数据说明游离的TSHR-A亚基具有更强的免疫原性,相比TSHR全长能更有效的诱导小鼠GD的发病,具有更高的造模成模率。
· 维真生物Ad-TSHR现货 ·
人源TSHR基因腺病毒现货,滴度高,周期短,帮助建立免疫诱导的甲亢动物模型,助力甲亢研究!
参考文献:
1. Chu YD, Yeh CT. The Molecular Function and Clinical Role of Thyroid Stimulating Hormone Receptor in Cancer Cells. Cells. 2020 Jul 20;9(7):1730.
2. McLachlan SM, Rapoport B. A transgenic mouse that spontaneously develops pathogenic TSH receptor antibodies will facilitate study of antigen-specific immunotherapy for human Graves' disease. Endocrine. 2019 Nov;66(2):137-148.
3. Chen CR, Pichurin P, Nagayama Y, Latrofa F, Rapoport B, McLachlan SM. The thyrotropin receptor autoantigen in Graves disease is the culprit as well as the victim. J Clin Invest. 2003 Jun;111(12):1897-904.
4. 覃海知,黄一薇,刘强,李承铉,李海洋,谢春光. 以 Ad-TSHR-289 构建 Graves 病动物模型的研究进展. 辽宁中医杂志2017年第44卷第7期 .
 当前位置:首页 > 新闻中心 > 新品发布
当前位置:首页 > 新闻中心 > 新品发布