 当前位置:首页 > 研究领域 > 消化系统
当前位置:首页 > 研究领域 > 消化系统
| 文章标题 | RNF115 upregulation by YBX1-dependent m5C modification promotes hepatocellular carcinoma progression |
| 发表期刊 | npj Precision Oncology (IF 8.0) |
| 合作客户 | 四川大学华西医院唐红/白浪研究团队 |
| 感染细胞 | Hep3B和Huh7细胞 |
|---|---|
| 病毒产品 | Lv-RNF115、Lv-shRNF115(3保1) |
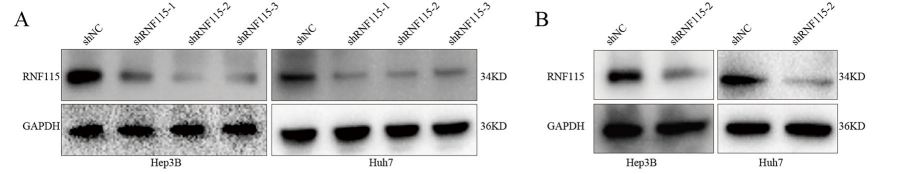
肝细胞癌(HCC)是全球第三大致癌相关死亡原因,现有治疗手段效果有限,5年生存率低,亟需阐明其发病分子机制并寻找新的治疗靶点。m5C作为一种重要的RNA修饰,通过甲基转移酶、去甲基化酶和阅读蛋白调控基因表达,其中阅读蛋白YBX1在多种癌症中具有致癌作用,但它在HCC中通过m5C修饰调控靶基因的具体机制尚不明确。
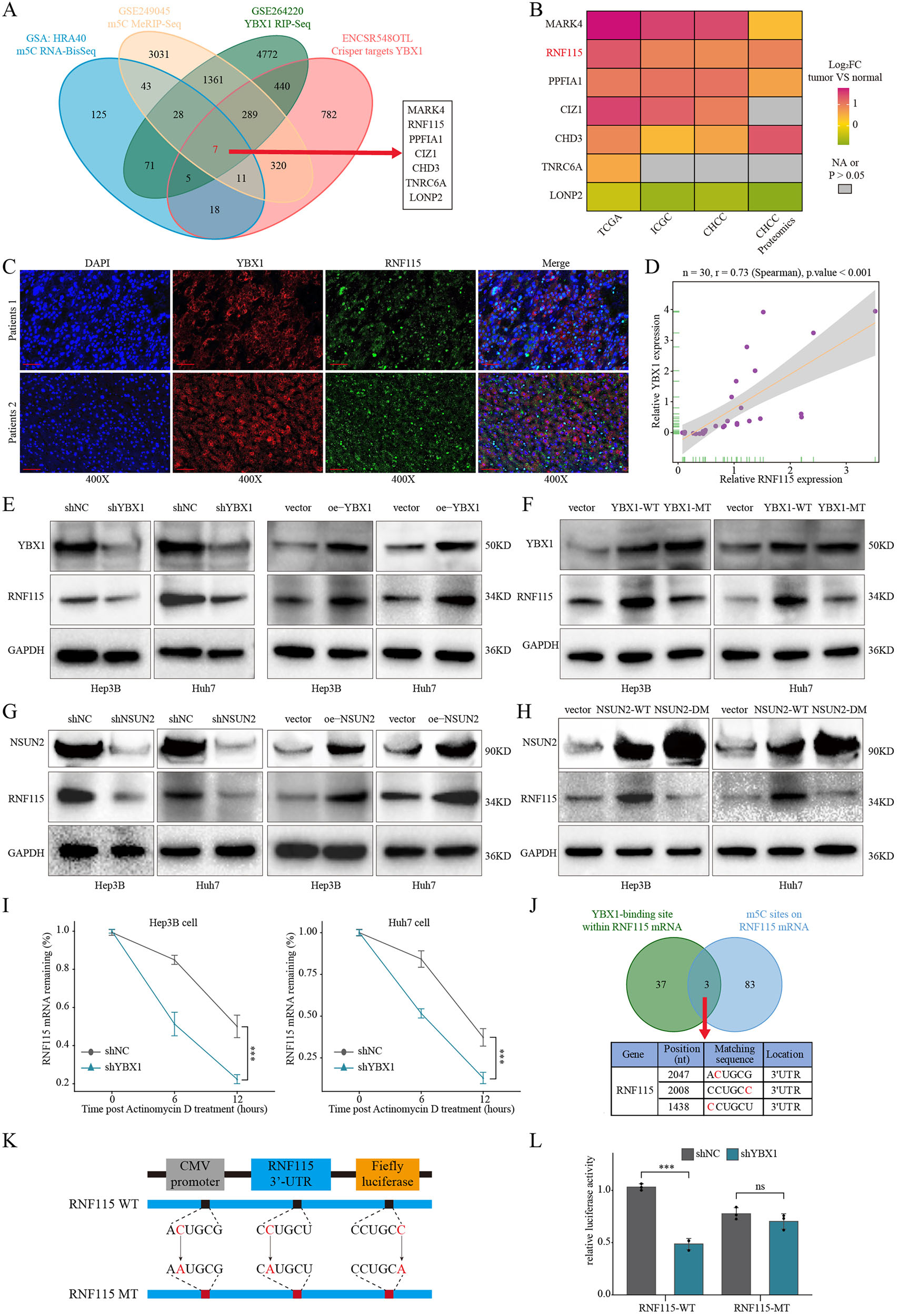
转录组水平m5C图谱分析显示,HCC组织与癌旁组织的m5C修饰模式存在显著异质性,差异甲基化基因广泛分布于除Y染色体外的所有染色体。此外,m5C相关调控因子YBX1在晚期HCC中表达升高,且高表达与患者不良预后密切相关。进一步通过功能丧失和功能获得实验证实YBX1促进HCC细胞增殖、迁移和侵袭。研究团队整合m5C MeRIP-seq、YBX1 RIP-seq 等多组学数据,RNF115被鉴定为受m5C依赖的YBX1直接调控靶基因。分析发现RNF115在HCC中的mRNA和蛋白水平均显著过表达,其表达与YBX1、NSUN2呈正相关,免疫荧光染色进一步验证了YBX1与RNF115蛋白的强相关性。机制上的探索证实,YBX1结合RNF115 mRNA 3' UTR的m5C修饰位点,增强其mRNA稳定性和翻译效率,从而上调RNF115蛋白表达。
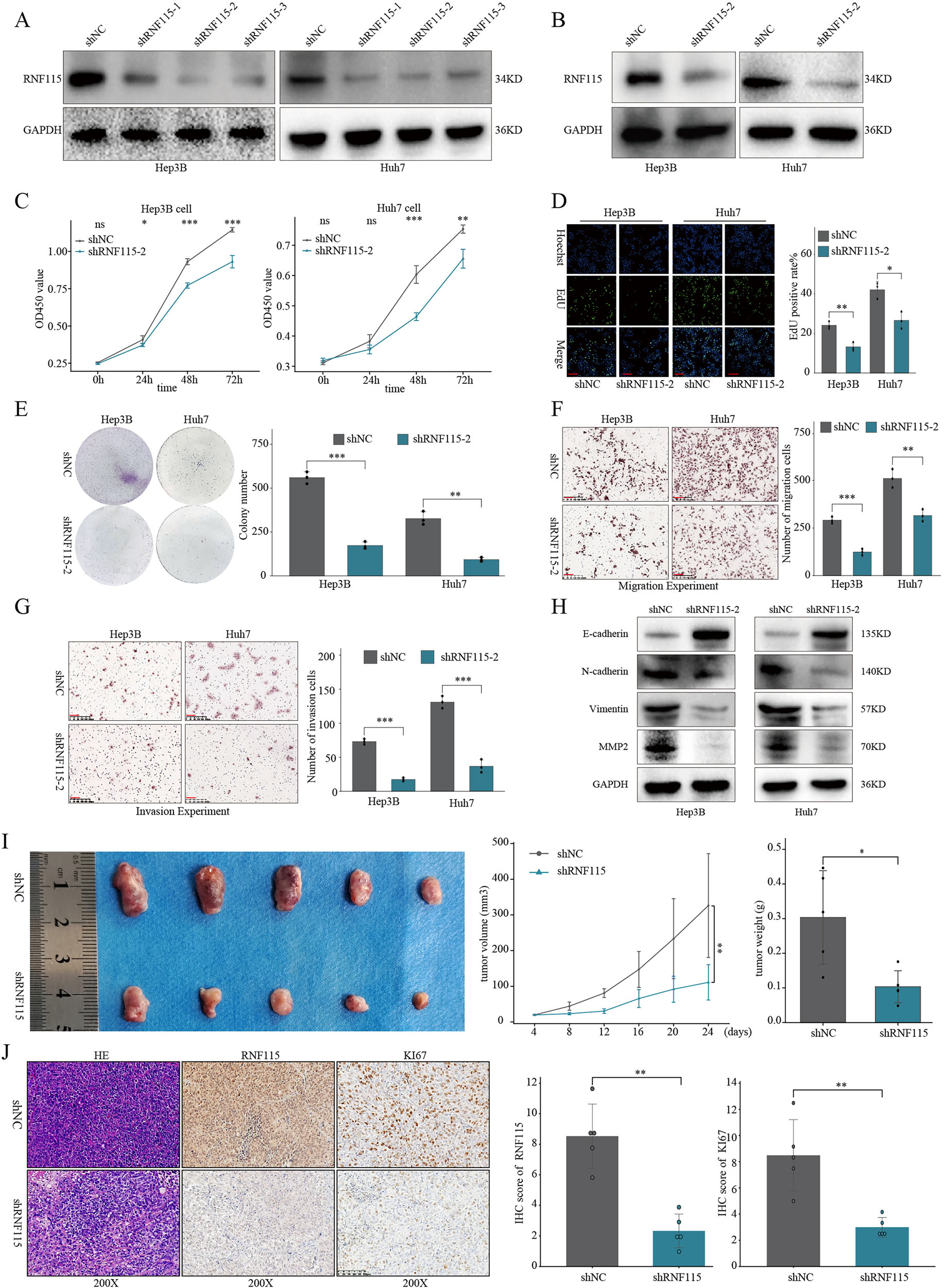
临床数据显示,RNF115在HCC组织中高表达,与晚期BCLC分期、较大肿瘤尺寸、高 PIVKA-II水平、复发转移及不良预后相关,是HCC的独立预后风险因子。利用慢病毒载体敲低RNF115可显著抑制HCC细胞增殖、迁移和侵袭能力,并下调间质标志物表达,上调上皮标志物表达。通过皮下注射shRNF115或shNC感染的HCC细胞建立了异种移植小鼠模型,得到了与体外一致的研究结果,表明RNF115可能增强HCC的恶性表型。随后的功能拯救实验确认了YBX1通过RNF115促进HCC恶性表型;进一步的探索证实YBX1通过上调RNF115激活PI3K/AKT信号通路,进而促进HCC进展,使用AKT抑制剂MK-2206可逆转RNF115过表达引起的促增殖效应。
本研究揭示了 YBX1/m5C-RNF115轴通过激活PI3K/AKT信号通路,驱动HCC进展的关键机制。研究结果不仅突显了该调控轴在HCC发病机制中的核心作用,也彰显了其作为治疗靶点的潜力。靶向YBX1/m5C-RNF115轴,无论是单独干预还是与PI3K/AKT通路抑制剂联用,为开发更有效的HCC治疗策略提供了极具前景的新方向。
备案号:鲁ICP备13011878号 网址:www.wzbio.com.cn









