 当前位置:首页 > 研究领域 > 其他
当前位置:首页 > 研究领域 > 其他
文章标题:IL7R Remodels Immunosuppression Tumor Microenvironment and Promotes Macrophage Polarization by Regulating NF-κB/CXCL1 Axis in Ovarian Cancer
发表期刊:Cell Death & Disease (IF 9.6)
合作客户:南京医科大学第一附属医院程文俊\张林团队
| 基因信息 | IL7R:循环白细胞介素7受体 |
|---|---|
| 病毒产品 | Lv-shIL7R、Lv-NC |
| 实验细胞 | 卵巢癌细胞OVCAR3 |
| 感染时间 | 48h |
在卵巢癌微环境中,肿瘤相关巨噬细胞(TAM)的极化与免疫抑制表型密切相关。尽管循环白细胞介素 7 (IL-7) 水平升高与不良预后相关,但这种关联背后的调节机制仍不完全清楚。在这项研究中,作者阐明了 IL7R 信号如何介导卵巢癌细胞和巨噬细胞之间的串扰,以维持免疫抑制肿瘤微环境 (TME) 的稳态。
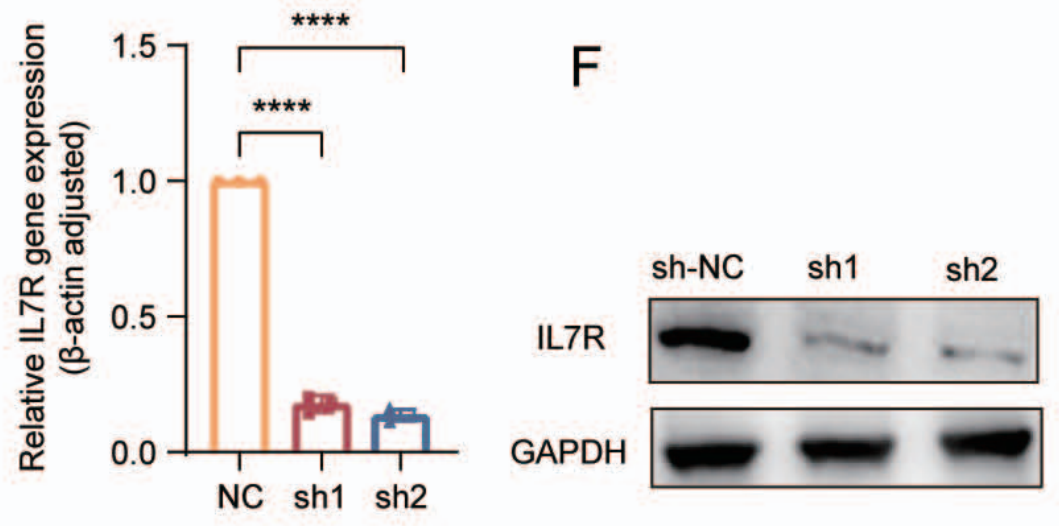
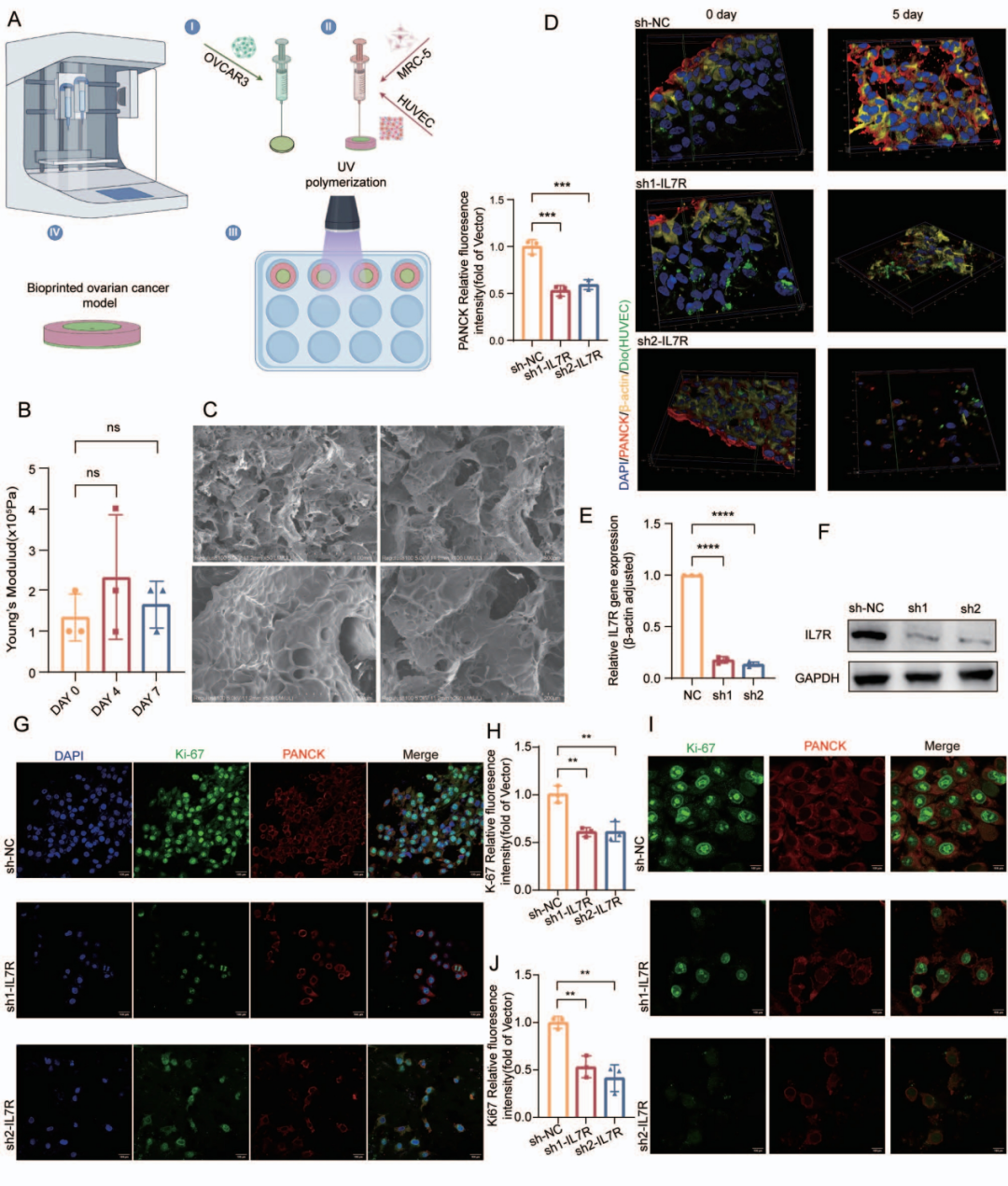
作者发现IL7R信号传导对于卵巢癌细胞的致瘤性和腹膜内传播至关重要,为了更好地重现肿瘤-基质相互作用,作者开发了3D生物打印技术构建肿瘤-基质共培养模型:核心区域为包裹卵巢癌细胞的水凝胶,外周为血管内皮细胞与成纤维细胞混合基质,模型力学性能稳定,细胞存活率超90%,可有效模拟肿瘤与微环境的空间交互。免疫荧光染色显示PANCK阳性肿瘤细胞和DiO预标记的HUVEC之间存在清晰的空间边界。为了研究IL7R的功能,使用Lv-shRNA建立了稳定的IL7R敲低卵巢癌细胞系,这些IL7R敲低细胞与基质成分联合生物打印,构建3D肿瘤基质模型。共培养五天后,IL7R敲低显著抑制细胞增殖。肿瘤-基质界面的动态跟踪表明,IL7R敲低缩短了肿瘤细胞从打印边界到基质的迁移距离。机制研究发现IL7R信号传导通过NF-κB/CXCL1轴促进巨噬细胞向免疫抑制表型极化,极化的巨噬细胞进一步增强肿瘤细胞的增殖和侵袭,从而形成肿瘤免疫反馈回路。
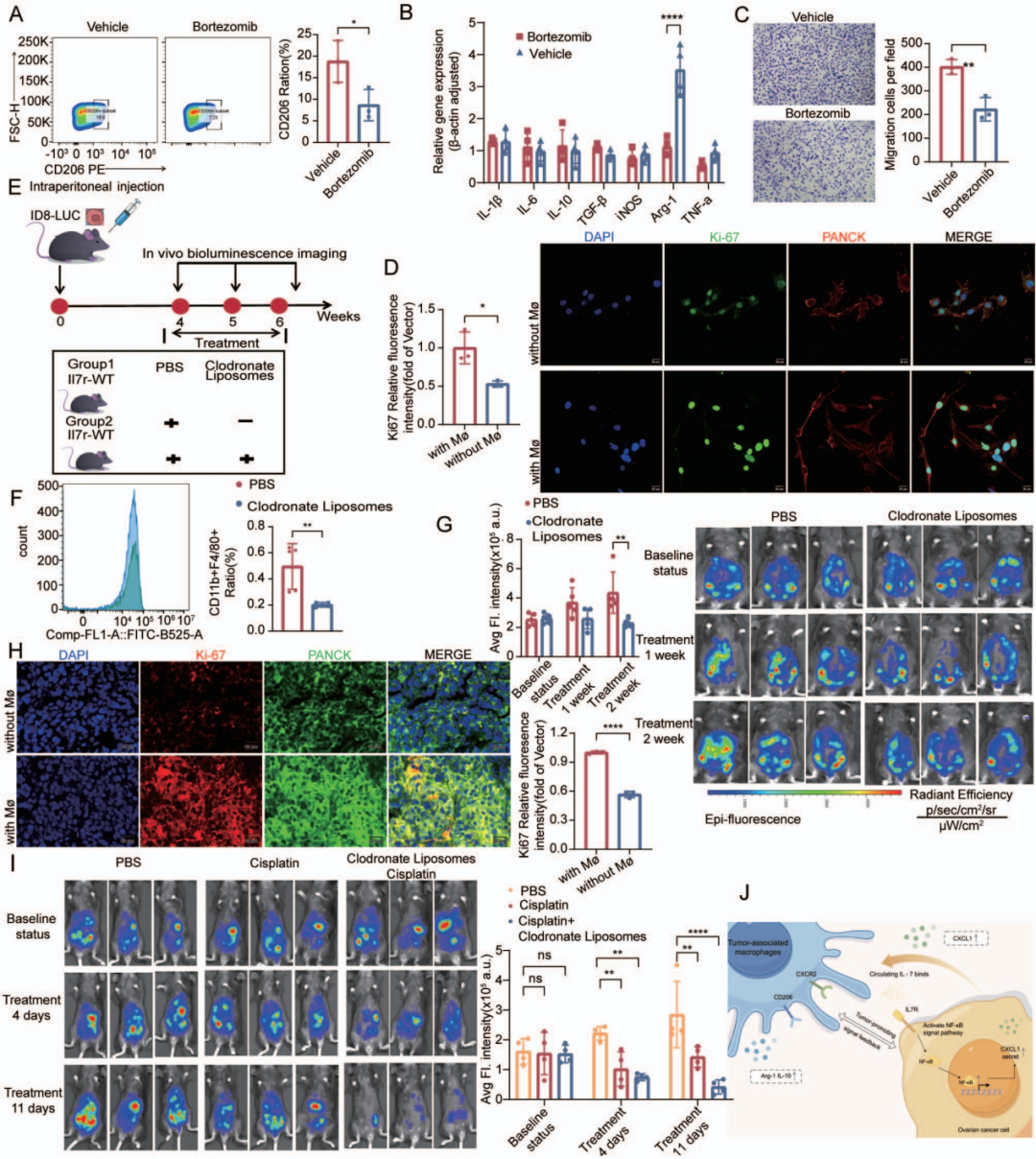
为了探讨巨噬细胞极化对肿瘤细胞恶性行为的反馈调节,作者采用3D生物打印技术构建肿瘤细胞与巨噬细胞的共培养体系。发现免疫抑制性极化巨噬细胞显著促进OVCAR3肿瘤细胞的增殖,表明免疫抑制TAM可以促进卵巢癌的进展。此外在小鼠移植模型中,氯膦酸钠治疗导致脾脏F4/80+CD11b+巨噬细胞比例显著减少。连续体外荧光成像显示,巨噬细胞耗竭导致肿瘤负荷显著减少,同时腹膜转移病灶数量和腹水量减少。此外,巨噬细胞耗竭后,肿瘤细胞中Ki67的表达下调。表明TAM促进肿瘤生长,而当TAM耗尽时,肿瘤生长受到抑制。鉴于巨噬细胞靶向治疗可以延缓小鼠卵巢癌的进展,作者进一步评估了巨噬细胞靶向治疗是否可以增强卵巢癌化疗的抗肿瘤疗效。结果显示,与PBS对照组和单药治疗组相比,氯膦酸钠脂质体与顺铂联合治疗显著抑制肿瘤生长速度。
本研究阐明了IL-7/IL-7R轴在卵巢癌微环境中的作用,并将肿瘤细胞中的IL-7R表达确定为调节IL-7信号传导的关键靶标。IL-7R介导的机制发挥双重促肿瘤作用:促进肿瘤细胞增殖和转移,以及重塑免疫微环境。这些发现不仅确立了IL-7R作为卵巢癌进展的驱动因素,还提供了IL-7如何通过促进肿瘤进展导致不良预后的新见解。
备案号:鲁ICP备13011878号 网址:www.wzbio.com.cn









